相信對很多神經科醫師而言,PART(Primary age-related tauopathy, PART)似乎只是個教科書上看到過的名詞,對它臨床上的基本特徵並不清楚,對病理表現只有模糊的概念。這篇文章對PART進行了全面的病理解剖研究,並納入了廣泛的年齡層,包括許多相對年輕和健康的受檢者。這使得研究結果更能反映PART在普通人群中的盛行率,挑戰了以往主要集中在老年病例的研究結果。
重點提問
研究人員如何進行這項研究?使用了哪些方法和數據?
PART 在那個年齡層盛行率最高?這些發現與之前的研究有何不同?
在年長的 PART 病例中,觀察到了哪些共病症?這些共病症對 PART 的臨床表現有何影響?
基於這些研究結果,作者對 PART 的診斷標準提出了哪些建議?
Prevalence and clinicopathological features of primary age-related tauopathy (PART): A large forensic autopsy study
文獻出處
背景
定義與特徵:PART是一種以神經纖維纏結(NFTs)為特徵的病理狀態,類似於阿茲海默症(AD),但沒有類澱粉蛋白-β(Aβ)斑塊的病理變化。好發於老年人,過去曾被稱為「僅有纏結的失智症 tangle-only dementia」、「神經纖維纏結型老年失智症 senile dementia of the NFT type」或「以纏結為主的老年失智症 tangle-predominant senile dementia」。
診斷標準:
- 明確Definite PART(D-PART):無Aβ斑塊(Braak NFT階段I-IV,Thal階段0)。
- 可能Probable PART(P-PART):少量Aβ斑塊(Braak NFT階段I-IV,Thal階段1-2)。
- 排除其他tau蛋白病變:如進行性核上性麻痺(PSP)、皮質基底核退化症(CBD)和慢性創傷性腦病。
- AGD的模糊性:是否將嗜銀顆粒病(AGD)排除在PART之外仍未明確,造成了一些混淆。
與阿茲海默症的區別:
- 臨床表現:PART的認知障礙通常不存在或比阿茲海默症輕微,患者年齡相對較大,且失智症進展較慢。
- 遺傳因素:阿茲海默症與載脂蛋白E(APOE)ε4基因有關,而PART與APOEε2基因有關。MAPT基因的H1單倍型是PART、阿茲海默症和其他四重複tau蛋白病變的共同風險因素。
- 神經病理學:阿茲海默症病例的海馬CA1和CA2區域的tau蛋白病理比PART病例更嚴重,但尚無明確的標記來區分PART和阿茲海默症。
研究目的
- 過去針對PART的研究樣本數有限,且主要集中在老年族群,對於年輕族群的PART了解不足。
- 本研究透過分析大量40歲以上的法醫病理解剖案例,深入探討PART的臨床病理特徵,期望能為PART的定義帶來新的見解。
研究方法
研究對象
- 總體案例數: 1589例,Department of Legal Medicine, University of Toyama (Toyama, Japan),
- 年齡:介於40至101歲之間,平均年齡為70.2歲。
- 性別分佈: 男性954例,女性635例。
- 年齡分佈: 大多數患者年齡在70多歲(404例),90歲及以上的群組案例數最少(83例)。
- 死亡原因: 自然死亡393例,意外創傷死亡735例,自殺或他殺445例,死因不明16例。
- 臨床病史: 172例(10.8%)有失智症,228例(14.3%)有精神科就診史。
- 排除標準
- 年齡小於40歲
- 嚴重損傷
- 死後變性 post-mortem degeneration(例如液化妨礙組織學分析)
- 大面積舊梗塞(>1 cm)
- 多發性腔隙超過三個腦標本
- 資料來源
- 家屬和警方調查記錄
- 主治醫師提供的醫療記錄(如有就醫史)
組織採樣與病理評估
- 腦組織固定: 所有腦部樣本均在20%緩衝福馬林中固定2至4週。
- 常規取樣部位: 包括額葉、顳葉、基底核和中腦等。
- 切片與染色:
- 所有切片在染色前均進行切割,染色方法包括Luxol fast blue和hematoxylin and eosin (LFB-HE)、Gallyas–Braak和Holzer染色。
- 免疫組織化學染色: 在所有案例的額葉、顳葉、基底神經節和中腦樣本中,進行常規免疫組織化學染色,以檢測磷酸化tau蛋白、磷酸化α-突觸核蛋白、TDP-43、膠質纖維酸性蛋白和Aβ。
- 陽性結果的進一步染色: 如果在初步免疫組織化學染色中檢測到陽性結果,則對後續切片進行額外的染色程序,包括對AT8陽性案例進行三重複tau蛋白和四重複tau蛋白的染色。
- 病理分期:
- NFTs:依據改良的Braak分期評估NFT負擔。
- 老年斑密度:根據CERAD標準評估。
- 腦內老年斑範圍:根據Thal等人標準評估。
- AD相關神經病理變化:依據NIA-AA指南分為四類。
- 路易氏體失智症病變:依據第三版共識Third Consensus Guidelines for Dementia with Lewy Body,。
- 巴金森病相關病理:依據α-突觸核蛋白免疫組織化學染色確定Braak分期。
- 銀染顆粒:使用Gallyas–Braak染色檢測。
- AGD病理分期:使用Saito等人分期系統評估。
- PSP:使用NINDS標準進行神經病理學診斷。
- TDP-43蛋白病變:依據AD分期和FTLD-TDP病理分類系統評估
診斷分類
- PART:
- Braak NFT階段 I-IV
- 無或少量Aβ病理
- 無其他tau蛋白病變
- 排除PSP或CBD案例
- 排除有argyrophilic grain disease (AGD) 的案例
- 根據Aβ的存在與否,分為P-PART和D-PART
- D-PART: definite PART, 符合 PART 標準且無 Aβ 病理
- P-PART: Possible PART, 符合 PART 標準且有 Aβ 病理
- AGD+PART: 符合PART標準且同時患有AGD的案例
- PART-C: 符合PART標準,但同時患有α-突觸核蛋白病變和/或TDP-43蛋白病變的案例
- pure PART: 符合PART標準,且無α-突觸核蛋白病變或TDP-43蛋白病變的案例
- control: AD相關病理,Braak NFT階段 < I,Thal 0,無其他共病病理
- AD: 符合NIA-AA指南中”高”級別的受試者
分析方法
- 連續變量: 使用 Mann–Whitney U 檢驗評估差異。
- 序數變量: 使用 Fisher 精確檢驗進行分析。
- 多重比較校正: 應用 Bonferroni 校正。
- 統計軟體: 使用 SPSS Statistics 26 和 JMP 14.3 進行分析。
結果
PART的流行病學分析
診斷分類
- PART: 從1589例中,排除控制組、AD、超出PART標準的AD相關病理、PSP或CBD、AGD+PART,剩餘719例(45.2%)被分類為PART。
- PART 分為兩組:
- PART-C: 90 例 (5.7%),合併 α-突觸核蛋白病變或 TDP-43 蛋白病變,其中大多數 (86 例,95.6%) 合併路易氏體病理
- pure PART: 629 例 (39.6%),無上述合併症
- D-PART: 469 例 (29.5%),符合 PART 標準且無 Aβ 病理
- P-PART: 250 例 (15.7%),符合 PART 標準且有 Aβ 病理。
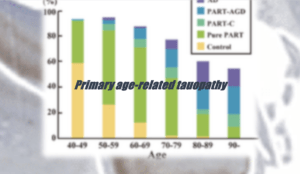
年齡分佈
- AGD+PART: 隨年齡增長比例增加,90歲以上佔比最高(21.7%)。
- pure PART: 50多歲和60多歲佔比最高(分別為58.5%和58.7%),之後逐漸下降,90歲以上佔比為15.7%。
- AD和PART-C: 隨年齡增長比例增加。
- AD在80歲以上達到峰值(20.0%),90歲以上佔比為14.5%。
- PART-C在70多歲達到峰值(8.5%),80多歲下降至3.7%,90歲以上回升至9.6%。
- D-PART和P-PART:
- D-PART: 50多歲佔比最高(53.0%)。
- P-PART: 60多歲佔比最高(23.6%)。
- 整體PART: 60多歲佔比最高(65.5%)。
- D-PART和P-PART在80多歲前下降,90歲以上再次上升。
- 整體PART在80多歲佔比為21.5%,90歲以上上升至25.3%。
性別差異
- 整體 PART 盛行率: 在 60 多歲之前保持相對穩定
- 70 多歲: 女性盛行率顯著下降,男性 232 例 (59.1%),女性 178 例 (46.6%)
- 90 多歲: 比例趨於相等,男性 27 例 (25.9%),女性 56 例 (25.0%)
- P-PART/D-PART 比例:
- 男性: 隨年齡增長而增加,從 40 多歲的 0.15 增加到 90 歲以上的 2.50
- 女性: 從 40 多歲的 0.08 逐漸增加到 80 多歲的 1.57,然後在 90 歲以上下降到 0.75.
AD 相關病理隨年齡和性別的進展
- 病理階段隨年齡增長而增加: Braak NFT 分期、Thal 分期和 CERAD 分期在男女兩性中均隨年齡增長而單側增加,直到 80 多歲。
- 女性案例增加速度更快: 女性案例在 70 多歲時 CERAD 分期升高,且所有分期在 80 多歲時顯著高於男性。
- 90 歲以上的變化:
- 女性案例: 所有分期在 90 歲以上達到高峰後下降
- 男性案例: 所有分期在 80 多歲開始趨於平穩
- 90 歲以上所有分期無顯著性別差異
PART 的臨床特徵
- pure PART 與控制組在失智症、精神科就診史或死因方面無顯著差異
- PART-C 組自殺率顯著高於 pure PART (p < 0.05)
- AGD+PART:
- 自殺率顯著高於控制組 (p < 0.05)
- 精神科就診率較高 (p < 0.01)
- 與 pure PART 相比,失智症更頻繁 (p < 0.01),自殺率更高 (p < 0.05),自然死亡率更低 (p < 0.01)
D-PART 和 P-PART 的比較
- P-PART:
- 年齡較大
- 更可能患有失智症
- 高 Braak NFT 分期和合併突觸核蛋白病變的頻率顯著高於 D-PART
調整年齡、性別和共病情況後分析結果:
- P-PART 和 D-PART 在臨床表現上無顯著差異
- P-PART:
討論
以下是為了能夠滿足段落所需的長度而定義的無意義內文,請自行參酌編排。
研究特色:此研究全面調查了 PART 的流行病學,包含 40 歲以上的法醫解剖案例,提供了關於 PART 合併症臨床意義的新觀點,有助於未來改進 PART 的診斷標準。
PART 盛行率
- 80 歲以上個體的 PART 盛行率 (22.1%) 與先前主要病理隊列的研究結果基本一致。
- 較年輕受試者 (50-70 歲) 的 PART 盛行率 (59.3%) 高於許多先前病理解剖隊列的研究,僅有 Braak 等人在解剖部門進行的研究報告的盛行率與本研究非常相似。
PART 診斷標準的反思
- 目前 PART 診斷標準基於 PART 主要發生在老年人的假設。
- 此研究中,較年輕 (小於 70 歲) 且符合 PART 標準的案例比例相對較高。
- 控制組、PART 組和 AD 組的平均年齡隨著 AD 相關病理的進展而增加。
- 嚴重 AD 病理的案例比例在 80 多歲達到高峰,在 90 歲及以上下降。
- 目前的 PART 診斷僅基於病理發現,理想的 PART 概念應考慮到 Aβ 病理達到平穩期後,AD 相關病理在生命晚期持續為 PART 病理。
- 可能需要設定年齡限制,並盡可能將未來可能發展為 AD 的個體排除在 PART 診斷標準之外。
- 80 歲可能是一個合理的 cutoff 年齡,因為本研究中符合 PART 標準的案例比例在 80 多歲下降,且 Aβ 的增加也在 80 多歲趨於平穩。
PART 的性別差異
- 先前報告顯示女性更容易發生 PART,但本研究隊列中沒有明顯的整體性別差異。
- 按年齡分析,70 多歲男性的 PART 盛行率高於同齡女性。
- 由於女性壽命普遍較長,在老年患者較多的隊列中,女性可能更容易被評估為易受 PART 影響。
- 需要進一步研究以確定 PART 是否存在性別差異,以及是否應將其反映在其診斷標準中。
共病病理發生率:
- 本研究顯示,符合 PART 標準的案例中,共病病理發生率在老年人中較高,年輕人中較低,這與先前研究一致。
- 在目前的 PART 標準中,路易氏體病變被認為是最常見的共病病理,但本研究發現 AGD 的共病率更高。
共病症對臨床表現的影響:
- 先前研究:無合併症的 PART 患者沒有臨床症狀;合併症可能增加老年 PART 個體的失智症風險
- 本研究:AGD 個體的自殺、失智症和精神科就診率顯著高於無 AGD 個體。
建議:
- 為確認 PART 病變的臨床意義,可能需要排除許多共病病理,包括路易氏體病理、AGD、PSP 和 CBD。
- 年齡限制和排除共病病理可能會顯著減少 PART 診斷的案例數,但將提供更純粹的案例組,以便更深入地探索 PART 的精確臨床意義。
研究限制
- 法醫屍檢案例隊列存在案例偏倚,不能完全反映背景人群分佈
- 中年組別案例數量較多,男性比例較高,意外和自殺案例較多
- 為消除這些偏倚,對每個年齡組和性別分別進行評估
- 難以調整死因,但結果可能更準確地反映社區人群中 PART 的盛行率,因為納入了許多無基礎疾病的年輕受試者
重點問答
1. 研究人員如何進行這項研究?使用了哪些方法和數據?
- 研究人員對 1589 例年齡在 40 歲以上的法醫病理解剖病例進行了全面調查,以研究與年齡相關的主要原發性 tau 蛋白病變(PART)的特徵。
- 他們分析了這些病例的臨床和病理數據,包括年齡、性別、死因、過去病史、大腦重量、心臟重量、各種病理指標(如 Braak NFT 階段、Thal amyloid beta 階段、CERAD amyloid beta 階段等)以及合併症情況,以了解 PART 的患病率、合併症、臨床表現和診斷標準。
2. PART 在那個年齡層盛行率最高?這些發現與之前的研究有何不同?
- 研究發現 PART 的患病率在 60 多歲的人群中最高 (65.5%),然後隨著年齡的增長而下降,在 80 多歲的人群中降至最低 (21.5%)。
- 這與之前的研究結果不同,之前的研究主要集中在老年病例,認為 PART 的患病率隨著年齡的增長而增加。
3. 在年長的 PART 病例中,觀察到了哪些共病症?這些共病症對 PART 的臨床表現有何影響?
- 研究發現,許多 80 多歲的 PART 病例除神經原纖維纏結病理外,還伴有共病症,特別是路易體病理和嗜銀顆粒病 (AGD)。
- 共病症會影響 PART 的臨床表現,例如 PART-C(有合併症的 PART)患者,嗜銀顆粒病和路易體病理顯著增加了 PART 患者的失智症和自殺風險。的自殺率顯著高於純 PART 患者。
4. 基於這些研究結果,作者對 PART 的診斷標準提出了哪些建議?
- 基於研究結果,作者建議重新評估 PART 的概念和診斷標準,特別是在年齡限制和排除合併症患者方面。
- 放寬年齡限制:由於 PART 在相對年輕的個體中也很常見,作者建議取消或放寬當前的年齡限制(例如,將年齡限制從 80 歲放寬到 70 歲),以便更準確地診斷 PART。
- 排除共病症:由於合併症會顯著影響 PART 的臨床表現,作者建議在診斷 PART 時排除其他合併症,如路易體病理和嗜銀顆粒病。這將有助於確定純 PART 的臨床意義,並更好地了解 PART 本身對認知功能和行為的影響。
個人想法
- 繼Limbic-predominant age-related TDP-43 encephalopathy (LATE) 之後,又一個依大量病理資料可能要被重新定義的疾病。
- 在年齡上的發現確實大大的顛覆了之前的認知,從前總覺得PART的病人應該是年紀非常大的,這個擴大年齡層的病理研究卻發現在 50-70歲的族群中也有很大比例已出現了PART的病理變化。
- PART病人在 50-70歲這個年紀時可能臨床症狀並不明顯,所以並未納入之前以dementia為目的的研究中,以dementia 為目的的研究不僅收案年齡較大,能夠做到病理解剖的年齡也較大。很有可能PART的preclinical stage比阿茲海默症更長,活的更久,所以之前以dementia為主的研究認定PART是年紀大的病人較會有疾病。
- 如果PART在 50-70歲的族群就出現,那此疾病的病名還用 primary age-related tauopathy 合適嗎?還是又會出現新的疾病名稱了?