臨床上血液 p-tau217 已能高準確度偵測阿茲海默症病理, 但「病理存在」是否等於「症狀由阿茲海默症驅動」, 仍是臨床最棘手的問題。此篇研究以兩階段流程切入的方式進行,診斷標準則是採用IWG對AD建議的診斷方式(無症狀但有biomarkers 的人建議診斷為 at risk for AD 而非 AA 所建議的 preclinical AD ) 。
重要提問
Q1: 為什麼單一血液生物標記(p-tau217)無法準確診斷阿茲海默症,而需要開發序列式檢測策略?
Q2: eMTBR-tau243相比其他tau相關生物標記,為何能更精準地反映臨床症狀嚴重程度?
Q4:eMTBR-tau243 陽性的患者,認知退化速度與 tau 蛋白在大腦的擴散方式,與陰性患者有多大差距?
Q5:eMTBR-tau243 能否取代 tau PET 來識別高 tau 負擔患者?這對抗澱粉蛋白療法的病人選擇有何實際影響?
Q6:eMTBR-tau243 陰性的 p-tau217 陽性患者,究竟是「安全的」還是仍需密切追蹤的高風險族群?這個「灰色地帶」臨床應如何解讀?
Integration of plasma eMTBR-tau243 and p-tau217 in the diagnosis and stratification of Alzheimer's disease: a prospective cohort study
文獻出處
背景
- 阿茲海默症的病理可從兩個維度理解:生物學維度(Aβ 斑塊 + tau 纏結累積)與臨床維度(認知退化,與 tau 纏結高度相關)
- 現行生物標記分為兩類:
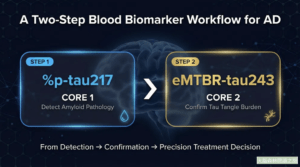
- Core 1 生物標記:反映 AD 病理是否存在(代表:p-tau217)
- Core 2 生物標記:反映 tau 纏結病理程度,用於生物學分期(代表:eMTBR-tau243)
- p-tau217 的根本限制:Aβ 病理在認知症狀出現前數年即已存在,導致許多無症狀或症狀另有原因的老年人同樣出現 p-tau217 升高,單靠 p-tau217 陽性無法判斷症狀是否由 AD 病理所致
- 研究假設:%p-tau217 用於確認 Aβ 病理存在;eMTBR-tau243 用於確認 AD 病理是否正在導致認知症狀
- 主要目的:驗證在 p-tau217 陽性患者中,加入 eMTBR-tau243 是否能改善確立型 AD 的分類精確度,並預測認知退化與 tau 纏結累積
研究方法
研究設計
- 前瞻性世代研究(prospective cohort study)
- 主要資料來源:瑞典 BioFINDER-2 研究,收案於兩個記憶門診
- 驗證資料來源:美國 Knight 阿茲海默症研究中心(ADRC) 隊列
- 收案期間:2017年5月18日至2023年9月8日;追蹤截止:2024年9月9日
收案條件
- 年齡 ≥ 40 歲
- 具有下列任一認知狀態:主觀認知衰退(SCD)、輕度認知障礙(MCI)、失智症
- 依認知測試結果及臨床評估連續收案,所有符合條件且具備完整資料者均納入
主要隊列(BioFINDER-2)
- 總人數:572 人
- SCD:142 人(25%)
- MCI:259 人(45%)
- 失智症:171 人(30%)
- 性別:女性 291 人(51%)、男性 281 人(49%)
- 確立型 AD:200 人(35%)
驗證隊列(Knight ADRC)
- 認知正常(CDR 0)至認知障礙(CDR 0.5–2)
- 主要分析使用認知障礙者 52 人(CDR 0.5:39 人、CDR 1:12 人、CDR 2:1 人)
- 另有部分患者具有神經病理解剖資料(n=80),用於 CERAD 斑塊評分與 Braak 分期驗證
血液生物標記
- 均使用質譜儀(mass spectrometry)進行定量分析
- %p-tau217:p-tau217 相對於非磷酸化np-tau217 的比值(unitless ratio)
- 陽性閾值:≥ 0.978(以 Gaussian mixture modelling 事前定義)
- eMTBR-tau243:以濃度表示(fmol/L)
- 陽性閾值:≥ 0.00132 fmol/L(同樣事前定義)
CSF 生物標記
- Aβ42 與 Aβ40:Elecsys 分析儀(Roche Diagnostics Cobas e601 全自動平台)
- Aβ 陽性定義:CSF Aβ42/Aβ40 比值 < 0.08
- α-synuclein:採用 SAA(seeding amplification assay)
影像生物標記
- Aβ PET:使用 [¹⁸F]flutemetamol;陽性閾值:≥ 20 centiloids
- Tau PET:使用 [¹⁸F]RO948;以小腦皮質作為參考區域
- 量化 Braak I–II、III–IV、V–VI 各分期區域的 SUVR
- 整體 tau 陽性定義:Braak I–IV meta-region SUVR ≥ 1.36
- TDP-43 MRI 特徵:下顳葉+中顳葉體積與海馬體積之比值(比值越大代表 TDP-43 病理可能性越高)
Knight ADRC 驗證隊列的影像方案
- Aβ PET:[¹¹C]PiB 或 [¹⁸F]florbetapir(陽性 ≥ 20 centiloids)
- Tau PET:[¹⁸F]flortaucipir;顳葉 meta-ROI 陽性閾值 1.32 SUVR
主要結果(Primary Outcome)
- 確立型阿茲海默症(Established AD):依 IWG(International Working Group)定義
- 需同時滿足:
- MCI 或失智症階段的 AD 臨床表型
- CSF 或 PET 確認 Aβ 陽性
- Tau PET(Braak I–IV 顳葉 meta-region)陽性
- 診斷過程不使用血漿生物標記資料,確保獨立性
- 需同時滿足:
次要結果(Secondary Outcomes)
- 認知測試縱向進展,包含:
- MMSE(整體認知)
- ADAS-recall(即刻與延遲回憶平均,反映記憶功能)
- TMT-A 及 TMT-B(處理速度與執行功能)
敏感度分析結果定義
- 可能型 AD(Probable AD):僅需 Aβ 陽性,不要求 tau PET 陽性(更寬鬆但較不特異的定義)
統計分析
- 非常態分布之生物標記資料以 log₁₀ 轉換處理
- 橫斷面分析:線性回歸評估生物標記濃度與神經病理特徵的關聯;以事前定義閾值計算診斷準確度、PPV、NPV;AUC 比較採用 DeLong’s test
- 縱向分析:線性混合效應模型(linear mixed effects models),調整年齡、性別、教育年數
- 偽時間分析(pseudotime):整合 CSF Aβ42/Aβ40 與 tau PET 為單一 AD 病理負擔分數(0–1),用於描述生物標記在病程中的動態軌跡
- 高 tau 負擔識別分析:以特定 NPV 目標值(85%、90%、95%)反推 eMTBR-tau243 閾值,計算對應準確度與 PPV
- 盛行率模擬:以 BioFINDER-2 的靈敏度與特異度,模擬 10–90% 盛行率下的 PPV 與 NPV 變化
- 統計顯著水準:p < 0.05;所有分析使用 R 4.4.3
研究結果
受試者基本特徵
- BioFINDER-2 共收案 572 人:SCD 142 人、MCI 259 人、失智症 171 人
- 確立型 AD:200 人(35%);女性 291 人(51%)、男性 281 人(49%)
- 在 p-tau217 陽性的 350 人中,依 eMTBR-tau243 分組特徵如下:
| 特徵 | eMTBR-tau243 陰性(n=156) | eMTBR-tau243 陽性(n=194) |
|---|---|---|
| 平均年齡 | 75.1 歲 | 73.5 歲 |
| 失智dementia比例 | 22% | 56% |
| MCI 比例 | 47% | 37% |
| SCD 比例 | 31% | 7% |
| APOE ε4 陽性 | 72% | 72% |
| Aβ 陽性 | 97% | 98% |
| Tau PET Braak I–IV 陽性 | 30% | 92% |
| 確立型definite AD | 23% | 84% |
| 其他神經退化診斷 | DLB 5%、血管性失智 5% | 幾乎為零 |
- 值得注意:兩組的 APOE ε4 盛行率相同(72%),白質病變體積亦無顯著差異,顯示 eMTBR-tau243 的分層效果並非由 APOE 基因型或腦血管因素所解釋
生物標記與 AD 病理負擔的動態關係(Pseudotime 分析)
- 以 AD pseudotime,0–1 代表病理負擔由低至高作為橫軸,描述各生物標記的異常出現順序:
- %p-tau217 與 Aβ PET:在偽時間約 0.25 以下(病理極早期)即開始上升,為最早出現異常的標記
- Tau PET Braak I–II:在早期即有輕微上升,但幅度有限
- Tau PET Braak III–VI 與 eMTBR-tau243:約從偽時間 0.50 起才明顯加速上升,代表其反映的是中至晚期的 tau 病理擴散
- 此動態軌跡在生物學上支持:
- %p-tau217 = core 1 標記(早期病理偵測)
- eMTBR-tau243 = core 2 標記(晚期、有臨床意義的 tau 纏結)
- 神經病理資料(Knight ADRC,n=80)進一步驗證:
- %p-tau217 在 CERAD 稀疏斑塊(sparse,p=0.035)及 amyloid Braak IV 期即已升高
- eMTBR-tau243 則需頻繁斑塊(frequent) 及 amyloid Braak V 期以上才顯著升高(p<0.0001),反映更嚴重的 AD 病理負擔
%p-tau217 單獨使用的診斷表現
- 350 名(61%)p-tau217 陽性患者中:
- 341 人(97%)確認有 Aβ 病理(CSF 或 PET)→ 確認 %p-tau217 對 Aβ 病理的 PPV 極高
- 222 名 p-tau217 陰性患者中,僅 32 人(14%)為 Aβ 陽性
- 然而,350 名陽性者中僅 199 人(57%)符合IWG definite AD → PPV 57%,偽陽性率達 43%
- 151 名偽陽性者的組成分析:
- 125 人(83%)tau PET 陰性(Braak I–IV)
- 63 人(42%)僅有 SCD,未達IWG denifite AD 臨床門檻
- 結論:%p-tau217 陽性代表「AD 病理已存在」,但不等於「AD 病理正在導致症狀」,單獨使用存在顯著臨床overdiagnosis 風險
eMTBR-tau243 在 p-tau217 陽性患者中的診斷表現(橫斷面)
- 350 名 p-tau217 陽性患者中,194 人(55%)同時為 eMTBR-tau243 陽性
- 以IWG definite AD 為參照標準,eMTBR-tau243 的診斷表現:
- 整體準確度:81%(95% CI 76–84)
- PPV:84%(95% CI 78–88)
- NPV:77%(95% CI 68–82)
- 靈敏度:82%(95% CI 76–87)
- AUC:0.88,顯著優於 %p-tau217 的 0.83(p=0.0038)
- 31 名偽陽性(eMTBR-tau243 陽性但非definite AD)的細節:
- 14 人為 SCD,未達臨床門檻,但其中 13 人(93%)的 tau PET Braak I–IV 為陽性,且縱向認知退化速度顯著快於 eMTBR-tau243 陰性的 SCD 患者
- 作者認為這群人可能是 AD 高風險族群(IWG 定義的 at-risk),而非真正的偽陽性
縱向認知退化分析
- 分析對象:p-tau217 陽性患者,依 eMTBR-tau243 狀態分組;平均追蹤 1.5 年(SD 0.6)
- 基線認知:eMTBR-tau243 陽性者在所有測試的基線分數均顯著較差
- 縱向退化(線性混合效應模型),eMTBR-tau243 陽性者退化速度顯著更快:
- MMSE:p<0.001
- ADAS-recall:p<0.01
- TMT-A:p<0.001
- TMT-B:p<0.001
- 敏感度分析(控制基線 tau PET Braak I–IV 後分析):
- ADAS-recall、TMT-A、TMT-B 的 eMTBR-tau243 效果幾乎完全衰減(p=0.77、0.74、0.083)
- MMSE 效果衰減 52%(β 從 –1.65 降至 –0.79)
- 確認 eMTBR-tau243 的認知預測力大部分透過 tau 纏結負擔所中介
- SCD 亞族群事後分析:eMTBR-tau243 陽性的 SCD 患者,認知退化速度在所有測試中均顯著快於陰性者,且基線 tau 負擔更高
縱向 Tau PET 累積分析
- Tau PET 第二次掃描距基線平均 2.1 年(SD 0.2)
- eMTBR-tau243 陽性者在基線時,所有 Braak 分期腦區的 tau 負擔均顯著高於陰性者
- 縱向 tau 累積差異:
- Braak I–II:兩組無顯著差異(最早期區域,兩組均已有一定程度累積)
- Braak III–IV:陽性者累積速度顯著更快(p<0.01)
- Braak V–VI:陽性者累積速度顯著更快(p<0.001)
- Braak I–IV 整體:陽性者累積速度顯著更快(p<0.01)
- 此結果符合 eMTBR-tau243 反映「tau 纏結已超越早期內嗅皮質限制、開始向新皮質擴散」的生物學假設
eMTBR-tau243 識別高 tau PET 負擔的表現
- 分析對象:p-tau217 陽性患者,評估 eMTBR-tau243 區分高 tau PET 與低/中等 tau PET 負擔的能力
- eMTBR-tau243 的整體 AUC:0.94(95% CI 0.92–0.96)
- %p-tau217 的 AUC:0.89(95% CI 0.86–0.93),兩者差異顯著(p=0.0003)
- 以不同 NPV 目標值設定閾值的結果比較:
| NPV 目標 | eMTBR-tau243 準確度 | eMTBR-tau243 PPV | %p-tau217 準確度 | %p-tau217 PPV |
|---|---|---|---|---|
| 85% | 85%(80–88) | 80%(68–90) | 83%(79–87) | 72%(58–83) |
| 90% | 87%(83–91) | 76%(65–85) | 83%(79–87) | 63%(53–72) |
| 95% | 87%(82–89) | 67%(57–75) | 78%(73–81) | 51%(43–59) |
- eMTBR-tau243 在所有 NPV 目標下的準確度與 PPV 均優於 %p-tau217,代表其作為高 tau 負擔篩查工具具有優越的臨床分層能力
敏感度分析與盛行率模擬
- 以 Probable AD 為結果(較寬鬆定義,僅需 Aβ 陽性):
- 350 名 p-tau217 陽性者中,245 人(70%)符合 probable AD(PPV 70%)
- 加入 eMTBR-tau243 後:PPV 升至 91%,NPV 降為 56%
- NPV 較低符合預期:probable AD 包含部分 tau PET 陰性患者,而 eMTBR-tau243 對此類患者偵測力本就有限
- 排除 SCD 患者後:
- PPV 仍顯著改善,但 NPV 由 77% 降至 66%,反映 SCD 族群中有較多真正的低 tau 負擔患者
- 盛行率模擬(10–90%):
- %p-tau217 單獨使用:靈敏度 99.5%、特異度 59.9%
- %p-tau217 + eMTBR-tau243:靈敏度 81.9%、特異度 79.4%
- 兩者組合的 PPV 在所有盛行率下均優於 %p-tau217 單獨使用,盛行率低於 50% 時 PPV 改善幅度超過 20%,臨床意義最為顯著
其他共病病理分析
- 在 p-tau217 陽性患者中,比較 eMTBR-tau243 陰性與陽性者的非 AD 病理特徵:
- TDP-43 相關 MRI 特徵(顳葉-邊緣系統比值):陰性者顯著較高(β=0.28,p=0.0022),提示 eMTBR-tau243 陰性的認知障礙患者有較高的 TDP-43 共病可能
- α-synuclein 播種試驗陽性率:陰性者數值較高(23% vs 17%),但未達統計顯著性
- 白質病變體積:兩組無差異
- 非 AD 失智症診斷:DLB、血管性失智、PSP 等均集中在 eMTBR-tau243 陰性組;陽性組幾乎無非 AD 診斷
Knight ADRC 驗證隊列結果
- 分析對象:52 名認知障礙患者(CDR 0.5–2)
- 27 人(52%)符合IWG definite AD;43 人(83%)為 p-tau217 陽性
- 在 p-tau217 陽性患者中:
- %p-tau217 單獨使用:PPV 63%(95% CI 44–74)
- 加入 eMTBR-tau243 後:準確度 91%(72–95)、PPV 93%(70–96)、NPV 88%(50–94)
- eMTBR-tau243 陽性者的 tau PET 負擔顯著更高(平均 SUVR 1.70 vs 1.22,p<0.0001)
- eMTBR-tau243 陽性者的認知功能顯著較差(MMSE 24.3 vs 28.1,p=0.0005)
- 盛行率模擬同樣確認:兩指標組合的 PPV 改善效果在 Knight ADRC 隊列中一致
討論
兩步驟序列診斷框架的臨床意義
- 作者提出可操作的兩步驟臨床工作流程(圖 2D):
- 第一步:以 %p-tau217 篩查,陰性者可高度排除 AD 病理(靈敏度近 99.5%)
- 第二步:%p-tau217 陽性者加測 eMTBR-tau243,陽性者判定為「Aβ+ tau+,AD 病理可能正在導致症狀」;陰性者判定為「Aβ+ tau–,症狀可能另有原因」
- 此框架的臨床價值:
- 減少偽陽性:避免將 Aβ 陽性但症狀非 AD 所致的患者誤判為確立型 AD
- 提升治療決策精確度:雙陽性患者(%p-tau217+ 且 eMTBR-tau243+)可視為抗澱粉蛋白治療的較佳候選者
- 識別需要深入鑑別的族群:單獨 %p-tau217 陽性、eMTBR-tau243 陰性者,應優先排除 TDP-43、Lewy body 等非 AD 病理,再考慮是否啟動 AD 標靶治療
eMTBR-tau243 陽性中的「偽陽性」再詮釋
- 31 名 eMTBR-tau243 偽陽性者(陽性但不符合IWG definite AD)中,14 名為 SCD
- 然而這 14 名 SCD 患者中,13 人(93%)有 tau PET 陽性,且縱向認知退化速度顯著快於 eMTBR-tau243 陰性的 SCD 患者,作者認為這群人應被視為 AD 高風險族群(IWG 定義的 at-risk for AD),而非真正的診斷錯誤
- 此族群因具有雙重生物學陽性(Aβ + tau 纏結)且認知仍在 SCD 階段,可能是早期抗澱粉蛋白介入的最合適目標族群
MTBR-tau243 用於治療分層的潛力
- 現有臨床試驗(TRAILBLAZER-ALZ 2)已證明高 tau 負擔患者對 donanemab 的反應顯著較差,效益風險比下降
- eMTBR-tau243 在識別高 tau PET 負擔方面的表現(AUC 0.94)優於 %p-tau217(AUC 0.89),在所有 NPV 目標閾值下 PPV 與準確度均更佳
- 治療分層應用情境:
- eMTBR-tau243 高值者:高 tau 負擔,抗澱粉蛋白治療效益可能有限,需審慎評估效益風險比
- eMTBR-tau243 低值但 Aβ 陽性者:tau 纏結尚未廣泛形成,可能是預防性抗澱粉蛋白介入的最佳時機窗口
eMTBR-tau243 陰性患者中的非 AD 病理訊號
- 在 p-tau217 陽性、eMTBR-tau243 陰性的患者中,研究者發現:
- TDP-43 相關 MRI 特徵顯著較高(β=0.28,p=0.0022)
- α-synuclein 陽性率數值較高(23% vs 17%),雖未達統計顯著
- 非 AD 失智症診斷(DLB、血管性失智、PSP)幾乎全集中在此族群
- 臨床建議:對於 %p-tau217 陽性但 eMTBR-tau243 陰性的患者,應優先進行非 AD 病理的完整鑑別診斷,再決定是否啟動 AD 標靶治療;若無法找到其他顯著病理,仍可考慮 AD 治療,但需審慎
研究限制
- 樣本族群侷限:主要樣本來自瑞典白人,為次級專家記憶門診的選擇性族群,盛行率(IWG definite AD 35%)可能不代表初級基層醫療或其他族裔的真實情況
- 驗證樣本規模偏小:Knight ADRC 驗證隊列僅 52 名認知障礙患者,雖結果一致,但統計信賴區間較寬
- 技術平台未轉化:%p-tau217 與 eMTBR-tau243 目前均需質譜儀,尚無全自動免疫分析平台,限制了臨床普及性;p-tau217 的免疫分析平台已在發展中,但 eMTBR-tau243 是否能達到相同表現仍未知
- 治療監測能力未驗證:eMTBR-tau243 與 tau PET 的縱向相關性雖強,但其作為抗澱粉蛋白或抗 tau 治療的監測指標,目前尚無任何資料支持
- 盛行率依賴性:任何生物標記的 PPV/NPV 均受盛行率影響,真實臨床環境(特別是基層醫療)的盛行率可能遠低於本研究設定,需以模擬結果謹慎推算
個人想法
- 這篇研究正面提出了無症狀的類澱粉陽性族群者的臨床表現和預後,真的如AA criteira所提類澱粉陽性就是AD嗎?如果類澱粉沈積只是其它疾病的共病呢?80多歲的患者,認知功能完全正常,卻在PET掃描中顯示Aβ陽性,究竟是否該被診斷為阿茲海默症?
- MTBR-tau243可能是tau-PET」平替的證據愈來愈強:eMTBR-tau243在識別高tau負擔患者中的AUC達0.94,幾乎與tau-PET的診斷價值相當,但成本低、易執行。
- eMTBR-tau243 陰性患者的處置,才是最需要臨床智慧的部分。研究顯示 eMTBR-tau243 陰性的 p-tau217 陽性患者,有較高的 TDP-43 特徵與 α-synuclein 陽性趨勢。這提醒我們:這群患者不是「排除 AD 就沒事」,而是需要更積極尋找其他病理的族群。 在臨床實務中,這意味著這類患者可能需要更完整的鑑別診斷工作,包括 DLB、FTLD-TDP、血管性認知障礙等的評估,而不是直接放行。
- 對 lecanemab 和 donanemab 的治療決策,這篇研究提供了迄今最具體的血液分層依據:目前抗澱粉蛋白藥物的核准條件仍以 Aβ 陽性為主要門檻,但 TRAILBLAZER-ALZ 2 已明確告訴我們高 tau 負擔患者療效較差,MTBR-tau243 的 AUC 達 0.94,在識別高 tau 負擔方面優於 p-tau217,若未來免疫分析平台成熟,這將是決定「現在治療」或「等待更好時機」或「可能需要anti-tau 治療」的重要血液工具
- 雙陽性的 SCD 族群,很可能是我們一直在尋找的「最佳治療窗口」: 事後分析中,%p-tau217 陽性且 eMTBR-tau243 陽性的 SCD 患者,93% 有 tau PET 陽性,且認知退化速度顯著更快。這群人在臨床上往往因為「症狀還不夠明顯」還未進入輕度認知障礙,而被排除在治療討論之外,但從生物學角度來看,他們恰恰是 tau 纏結剛開始擴散、Aβ 負擔尚在可干預範圍的族群。這提示我們,未來的治療時機討論必須從「症狀出現後」提前至「雙標記陽性但症狀尚輕」的階段。
重點問答
Q1: 為什麼單一血液生物標記(p-tau217)無法準確診斷阿茲海默症,而需要開發序列式檢測策略?
A:p-tau217 確實是目前最準確的血液 Aβ 病理篩查工具,靈敏度接近 99.5%,與 CSF 及 PET 的 Aβ 陽性高度一致。然而,Aβ 病理在認知正常的 80 歲長者中盛行率達 30%,代表許多「p-tau217 陽性」個體其實處於無症狀病理期,認知障礙可能另有原因(如 TDP-43、Lewy body、血管病變)。此外,在 p-tau217 陽性的患者中,如何進一步辨別哪些人的認知症狀確實是由阿茲海默症病理所驅動,也是另一個重要的臨床問題。
Q2: eMTBR-tau243相比其他tau相關生物標記,為何能更精準地反映臨床症狀嚴重程度?
Q3: 整合%p-tau217和eMTBR-tau243的兩步驟工作流相比單一檢測,診斷精確度具體改變了多少?數字背後反映的臨床意義是什麼?
Q4:eMTBR-tau243 陽性的患者,認知退化速度與 tau 蛋白在大腦的擴散方式,與陰性患者有多大差距?
A:縱向追蹤(平均 1.5 年)顯示,在 p-tau217 陽性患者中,eMTBR-tau243 陽性者在所有認知測試的退化速度均顯著較快:MMSE(p<0.001)、ADAS-recall(p<0.01)、TMT-A 及 TMT-B(p<0.001)皆呈現更陡峭的惡化曲線。Tau PET 縱向追蹤(平均 2.1 年)則顯示,陽性者在 Braak III–VI 區域的 tau 累積速度明顯更快,Braak I–II 最早期區域兩組無差異。這說明eMTBR-tau243特別能反映中晚期的tau聚集進展。即使只看那些只有主觀認知衰退的患者,eMTBR-tau243陽性組的認知衰退曲線依然更陡峭。eMTBR-tau243 對大部分認知豖能的預測效果在調整基線 tau PET 後幾乎完全衰減,確認其預測力主要是透過 tau 纏結負擔所中介。但加入tau PET 後eMTBR-tau243對MMSE衰退的預測效應雖然減弱了52%(β -0.79, p=0.018),但還是保留了一部分,這說明它的預測力在MMSE上不完全是因為反映tau病理負擔。
Q5:eMTBR-tau243 能否取代 tau PET 來識別高 tau 負擔患者?這對抗澱粉蛋白療法的病人選擇有何實際影響?
A:此研究結果在治療決策上所提出的建議為,在 p-tau217 陽性患者中,eMTBR-tau243 識別「高 tau PET 負擔」的 AUC 高達 0.94,顯著優於 p-tau217 的 AUC 0.89(p=0.0003)。以 NPV 90% 為目標時,eMTBR-tau243 的準確度 87%、PPV 76%,優於 p-tau217 的準確度 83%、PPV 63%。臨床意義在於:TRAILBLAZER-ALZ 2 等試驗已證明高 tau 負擔患者對抗澱粉蛋白治療反應較差,若能以血液 eMTBR-tau243 前篩,可避免高 tau 患者承擔 ARIA 風險卻獲益有限的治療,同時節省高成本 tau PET 檢查資源。
Q6:eMTBR-tau243 陰性的 p-tau217 陽性患者,究竟是「安全的」還是仍需密切追蹤的高風險族群?這個「灰色地帶」臨床應如何解讀?
A:這是研究中提到要謹慎解讀的「灰色地帶」。p-tau217 陽性、eMTBR-tau243 陰性者(n=156)被歸類為「Aβ 陽性但 tau 纏結尚不顯著」,研究者在此族群中確實發現較高的 TDP-43 相關 MRI 特徵及較多 α-synuclein 陽性趨勢,提示症狀可能另有病理根源。然而,這不等於可以安心排除 AD 風險——在 SCD 亞族群分析中,eMTBR-tau243 陽性的 SCD 患者 93% 有 tau PET 陽性,且認知下降速度顯著更快,顯示部分 eMTBR-tau243 陰性者仍可能處於病理早期的治療窗口。此外,eMTBR-tau243 目前仍依賴質譜儀平台、尚未自動化,也未在多元族裔族群中驗證,距廣泛臨床應用仍有待突破。
內容總整理(懶人包)
| 面向 | 內容 |
|---|---|
| 研究設計 | 前瞻性世代研究(BioFINDER-2)+獨立驗證(Knight ADRC) |
| 主要樣本 | 572 名記憶門診患者(SCD 142、MCI 259、失智症 171) |
| 驗證樣本 | 52 名認知障礙患者(Knight ADRC) |
| 主要結果定義 | Definite AD(IWG 標準:臨床症狀+Aβ 陽性+tau PET 陽性) |
| 兩步驟策略邏輯 | Step 1:%p-tau217 篩查 Aβ 病理 → Step 2:eMTBR-tau243 確認 tau 致病性 |
| 策略優勢 | PPV 從 57% 提升至 84%;盛行率低於 50% 時 PPV 改善幅度超過 20% |
| 驗證隊列一致性 | Knight ADRC:準確度 91%、PPV 93%、NPV 88% |
| 治療分層應用 | eMTBR-tau243 高值 → 高 tau 負擔 → 抗澱粉蛋白治療效益可能有限 |
| eMTBR-tau243 陰性的臨床意涵 | 需積極排除 TDP-43、Lewy body、血管性等非 AD 病理 |
| SCD 族群特殊發現 | 雙陽性 SCD 患者 93% 有 tau PET 陽性,認知退化顯著更快,為潛在早期介入目標 |
| 主要限制 | 樣本族群單一(瑞典白人)、eMTBR-tau243 尚無自動化平台、治療監測能力未驗證 |
| 臨床轉化關鍵障礙 | eMTBR-tau243 免疫分析平台尚未建立,目前無法在一般醫院常規執行 |
| 未來最重要研究問題 | eMTBR-tau243 能否作為抗澱粉蛋白治療反應的動態監測指標? |