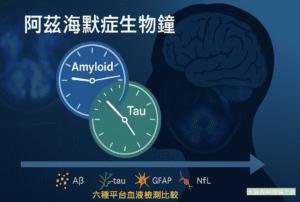
在阿茲海默症的早期診斷與追蹤中,生物標記的「出現時間點」具有關鍵意義。此研究運用類澱粉與tau PET作為時間對齊參考,首度描述出檢驗六種商用平台C2N、Fujirebio、ALZpath、Janssen、Roche、Quanterix血漿生物標記在時序上的差異,分析出生物指標,MRI,CDR-SB異常出現的順序地圖。
重點提問
Q1. 為何要用「類澱粉鐘」與「tau 鐘」對齊血漿指標?
Q2. 在類澱粉時間軸上,哪個指標最早異常?血漿還是PET?提早多少?
Q3. 在 tau 時間軸中,GFAP 與 p-tau 的先後順序透露什麼病理訊息?
Q4. 預測臨床症狀時,哪個里程碑最可靠?
Q5. 同一指標換檢測平台為何會改寫時間軸?臨床該如何解讀?
Timing of Changes in Alzheimer's Disease Plasma Biomarkers as Assessed by Amyloid and Tau PET Clocks
文獻出處
背景
既有證據與盲點
過去多數縱向研究僅將「類澱粉 PET 陽性」設為時間零點,推估血漿指標何時偏離;然而 AD 病程並非單向序列,tau 病理與星狀膠細胞反應可能獨立於 Aβ 動態,因此單一時標無法完整反映真實變化。臨床與試驗痛點
提早多久:醫師與試驗設計者需要知道每項血漿指標究竟領先影像與症狀多少年,才能鎖定「最佳預防窗」。
指標排序:缺乏同時整合 Aβ 與 tau 參考點的高解析度時間圖,難以準確分期或評估藥物反應。
研究目的
- 以 ADNI 784 例 Aβ PET 與 359 例 tau PET 縱向資料,建立兩條「生物鐘」── Amyloid-PET Clock 與 Tau-PET Clock──再將 292 名受試者的三次血檢對齊至雙時標;藉此:
精確量化 Aβ42/Aβ40、p-tau217、p-tau181、GFAP、NfL 何時首次異常;
檢驗六種商用平台(C2N、Fujirebio、ALZpath、Janssen、Roche、Quanterix)在時序上的差異。
解析哪一個里程碑(Aβ 或 tau 陽性年齡)最能預測臨床症狀。
預期貢獻
透過雙時標方法,本研究希望:為臨床提供可量化的「血漿-影像-症狀」對照年表,協助早期篩檢與個案分期;
為試驗端界定適切收案時間窗,並釐清不同平台在早期偵測上的優缺點;
進一步驗證 tau 病理在驅動認知衰退上的核心角色。
研究方法
整體設計
利用 Alzheimer’s Disease Neuroimaging Initiative (ADNI) 公開縱向資料庫,執行回溯性世代研究。
以 雙生物鐘架構(Amyloid-PET Clock、Tau-PET Clock)對齊血漿動態,並以 症狀鐘(臨床診斷轉折)作外部比對。
受試者與分組
影像母樣本:
Aβ PET:784 人;Tau PET:359 人。
包含認知正常(CU)、輕度認知受損(MCI)與臨床失智。
血漿樣本:292 人,每人 3 次血檢(基線+2 次後續)。
190 人屬 Aβ-PET 陽性,70 人屬 Tau-PET 陽性;80 名全程 PET 陰性的 CU 作「參考時間零」。
入選條件:≥1 次 PET 陽性掃描,完整血漿與 APOE 基因型;排除重大中風、腫瘤及 eGFR < 30 mL/min。
生物標記物測量
血漿生物標記物由六個平台測得:
Aβ42/Aβ40:C2N, Roche, Fujirebio, Quanterix
p-tau217 / %p-tau217 / p-tau181:C2N, ALZpath, Janssen, Roche, Fujirebio, Quanterix
GFAP, NfL:Roche, Quanterix
CSF 測值使用 Roche Elecsys® 系列(p-tau181、Aβ42、Total tau)
APOE 基因型亦一併檢測
影像與結構數據
類澱粉 PET(18F-Florbetapir)與 tau PET(18F-Flortaucipir)依 ADNI 標準化流程進行,計算 SUVR 與 Centiloid 值。
建立陽性門檻:
類澱粉 PET 陽性 SUVR = 0.78(≈26 Centiloid)
tau PET 陽性 SUVR = 1.41(限 mesial-temporal ROI)
結構性 MRI 由 FreeSurfer 自動分區,並計算 meta-ROI 的皮質厚度,經 ComBat-GAM 統一標準化處理。
神經心理與臨床評估
參與者接受完整臨床評估,包括旁證者訪談、神經理學檢查、CDR 與 CDR-SB 評估。
根據臨床診斷分為正常認知(CU)、輕度認知障礙(MCI)與失智(Dementia)。
MCI 或失智者進一步判斷是否屬於阿茲海默症(AD)或非AD病因。
症狀timeline以CDR>0, 且臨床診斷為MCI or dementia
| 平台 | 檢測項 | 技術 |
|---|---|---|
| C2N MS | Aβ42/40, %p-tau217 | 質譜 |
| Roche Elecsys | Aβ42/40, p-tau181, GFAP | ECLIA |
| ALZpath | p-tau217 | 高靈敏免疫化學發光 |
| Janssen | p-tau217, GFAP | Simoa |
| Fujirebio Lumipulse | Aβ42/40 | CLEIA |
| Quanterix Neurology 4-Plex | Aβ42/40, NfL, GFAP, p-tau181 | Simoa |
統計方法
Step 1:建鐘
對每位受試者多時點 SUVR 以 線性混合模型估坡度。
使用 廣義加乘模型 (GAM) 擬合非線性趨勢並積分,推算達陽性年齡。
Step 2:血漿對齊
以「距 Aβ-PET 陽性 X 年」與「距 Tau-PET 陽性 X 年」為自變項,對五大血漿指標建 GAMM (random intercept + spline)。
參考組 95 % CI 外即定義「首次異常」;曲線一階導數顯著離 0 點為「加速期」。
Step 3:症狀預測
線性回歸比較「Aβ-PET 年齡」vs「Tau-PET 年齡」對症狀年齡之 R²。
健度驗證:
1,000 次 bootstrapping 取「首次異常」95 % CI。
與 116 名 phenoconverter 真實數據比對(ρ = 0.96)。
敏感度分析:年齡、性別、APOE ε4 校正及「平台齊全」子樣本重跑。
- 以 eGFR、BMI、腦血管病灶作分層,檢視腎功能與共病對時序影響;結果僅 NfL 在 eGFR < 60 時延遲 1.3 年,其餘指標穩定。
研究結果
受試者概況
總樣本 784 人 (Aβ PET);359 人 (Tau PET)。
血漿樣本 292 人;平均年齡 73.9 ± 7.0 歲;女性 46%;APOE ε4 攜帶率 41%。
臨床分布:61.3% CU、36.0% MCI、2.7% AD 失智。
第一次血檢時Aβ-PET 陽性率 44.5%。
建立阿茲海默症 PET 時鐘模型
建構方法:以ADNI中從陰性轉為陽性的個案,根據其實際轉陽年齡與預測年齡高度相關(ρ=0.96),建構出 amyloid PET 時鐘與 tau PET 時鐘。
平均預測轉陽年齡:
類澱粉PET:66.6歲
Tau PET:73.7歲
臨床發病:81歲
模型結果:類澱粉與tau的堆積速度一致但個體差異大;tau PET 時點對發病年齡預測更具意義(R²=0.86)。
Amyloid PET Timeline
最早偏離:血漿 Aβ42/40(C2N、Roche)約在斑塊閾值前 8 年下降,比 CSF 與影像領先。
持續變化:CSF p-tau181/Aβ42、Aβ-PET、mesial-temporal tau-PET、皮質厚度、CDR-SB 全程呈顯著變動。
平台差異:Quanterix Aβ42/40 與部分 p-tau 指標明顯延遲 2–4 年,跨平台解讀須校正。
影像遞延:Temporo-parietal tau-PET 要到 +5.8 y 才開始上升,晚於內側顳葉。
末期指標:NfL 最後升高(+9 ~ +10 y),標誌晚期神經元損傷階段。
| 類別 | 指標 / 平台 | 首次異常時間點* (Aβ-PET 0 = 0) |
變化特徵 | 補充說明 |
|---|---|---|---|---|
| 類澱粉核心 | Aβ-PET SUVR | −5.9 y | 持續上升 | 190 位受試者,全程變化顯著 |
| CSF p-tau181/Aβ42 | −5.2 y | 持續上升 | 與 Aβ-PET 相近 | |
| 早期血漿 Aβ | C2N / Roche Aβ42/40 | −7.9 y | −7.9 – −7.1 y 降 → +11.5 – 13 y 平臺 | 超早期篩檢窗口 |
| Fujirebio Aβ42/40 | −5.8 y | 同上 | — | |
| Quanterix Aβ42/40 | −3.4 y | 同上 | 靈敏度最低 | |
| 血漿 p-tau | C2N %p-tau217 | −4.4 y | 全程上升 | 百分比檢測最早 |
| Roche p-tau181 | −2.9 y | 全程上升 | — | |
| ALZPath / Janssen p-tau217 | −3.9 – −3.2 y | 全程上升 | — | |
| Fujirebio p-tau217 | −1.5 y | 全程上升 | 最晚異常 | |
| Quanterix p-tau181 | ≈ 0 y | 全程上升 | 與閾值同步 | |
| GFAP(星狀膠細胞) | Roche GFAP | −3.9 y | 全程上升 | — |
| Quanterix GFAP | −3.5 y | |||
| Tau 影像 | Mesial-temporal tau-PET | 0 y | 全程上升 | — |
| Temporo-parietal tau-PET | +5.8 y | |||
| 結構 & 功能 | CDR-SB | 0 y | 功能↑ / 結構↓ | 功能量表 / 結構萎縮 |
| 皮質厚度 (Meta-ROI) | +2.9 y | |||
| 神經退化 | Plasma NfL | +9.2 – +10.5 y | 全程上升 | 最後異常 |
*負值:早於類澱粉 PET 陽性;正值:晚於類澱粉 PET 陽性。
Tau PET Timeline
Tau-PET 之前:Aβ-PET 與 CSF p-tau181/Aβ42 已異常(−8 ~ −7 y),GFAP 及血漿 Aβ42/40(質譜 / Roche)亦落在 −11 ~ −9 y 早期區段。
功能微損:CDR-SB 在 tau 0 −5.7 y 就開始爬升,顯示臨床細微變化可早於影像變化。
結構萎縮:皮質厚度在 −2.8 y 即低於參考組,但真正速率加快是 τ0 +0.5 y 之後。
平台落差:Quanterix Aβ42/40 僅在 τ0 附近短暫下降;Quanterix GFAP、NfL 更未呈顯著斜率,提醒跨平台時須調整解讀。
晚期指標:NfL 最後升高(+5 ~ +15 y),標記神經元損傷與臨床退化尾端。
Tau 時間軸(tau-PET 閾值 = 0)
| 類別 | 指標 / 平台 | 首次異常時間點* (tau -PET 0 = 0) |
變化特徵 | 補充說明 |
|---|---|---|---|---|
| Tau 核心 | 18F-FTP mesial-T tau-PET | −4.7 y | 全程上升 | 內側顳葉 |
| 18F-FTP TP tau-PET | −0.6 y | 0–5 y 稳定 → 之後上升 | tau 擴散較晚 | |
| Aβ-PET SUVR | −7.8 y | 全程上升 | 斑塊堆積 | |
| CSF p-tau181/Aβ42 | −7.4 y | 全程上升 | 液體 tau 活化 | |
| 早期血漿 Aβ | C2N Aβ42/40 | −9.3 y | 全程下降 | 與 Roche、GFAP CI 重疊 |
| Roche Aβ42/40 | −9.0 y | 全程下降 | — | |
| Fujirebio Aβ42/40 | −7.1 y | −0.8 ~ +4.4 y 顯著下降 | 區段較窄 | |
| Quanterix Aβ42/40 | −1.0 y | −1 ~ +6 y 下降 → +6 y 平臺 | 靈敏度最低 | |
| GFAP | Roche GFAP | −11.5 y† | 全程上升 | 星狀膠細胞最早訊號 |
| Quanterix GFAP | −10.0 y | 斜率不顯著 | 平台不敏感 | |
| 血漿 p-tau | Roche p-tau181 | −6.7 y | 全程上升 | — |
| Quanterix p-tau181 | −5.4 y | −5.4 ~ +3.6 y 上升 | +3.6 y 後趨平 | |
| ALZPath p-tau217 | −5.4 y | 全程上升 | — | |
| Janssen p-tau217 | −4.9 y | 全程上升 | — | |
| C2N %p-tau217 | −5.1 y | 全程上升 | 百分比法較早 | |
| C2N p-tau217 (濃度) | −4.7 y | −1 y 起才顯著 | 濃度法較晚 | |
| 功能 / 結構 | CDR-SB | −5.7 y | 全程上升 | 功能微損 |
| 皮質厚度 (Meta-ROI) | −2.8 y | +0.5 y 起速降 | 結構萎縮 | |
| 神經退化 | Roche NfL | +5.3 y | 全程上升 | 晚期損傷 |
| Quanterix NfL | +15.3 y | 斜率不顯著 | 最遲異常 |
*負值 = 早於 tau-PET 陽性;正值 = 晚於 tau-PET 陽性。
†Roche GFAP 點估 −11.5 y,但 95% CI 與 Aβ42/40(−9 ~ −7 y)重疊,未顯著早於 Aβ。
本表由 ChatGPT 依論文 Figure 4 與文字描述推算,供導讀參考。
症狀發病時間軸
最早偏離(-14 ~ -13 年)
全腦 Aβ-PET 與 CSF p-tau181/Aβ42 首先異常,標示「病理種子」已落地。
Roche、C2N 血漿 Aβ42/40 在同一時段即可偵測,適合社區超早期篩檢。
早期擴散(-12 ~ -9 年)
Mesial-temporal 及 TP tau-PET 於 −11.9、−11.7 年相繼升高;
血漿 p-tau217/181 與 GFAP 同步提升(−11.7 ~ -9.4 年),反映 tau 活化+星狀膠細胞反應。
Quanterix Aβ42/40 延後到 −8.4 年才異常 → 平台敏感度最低。
臨床前微損(-8.6 ~ -2 年)
功能量表 CDR-SB 變化點在 −6.2 年,MRI 皮質厚度 在 −2.1 年開始顯著下降。
血漿 Aβ42/40 降幅於 −0.8 年後趨平,各平台皆無後續顯著下降。
晚期指標
血漿 NfL 最後異常:Roche −4.3 年,Quanterix −2.9 年,代表神經元損傷階段。
症狀時間軸(Symptom Onset = 0)
| 類別 | 指標 / 平台 | 首次異常時間點* (Symptom 0 = 0) |
變化特徵 | 補充說明 |
|---|---|---|---|---|
| 影像 / CSF 核心 | Aβ-PET SUVR | −14.4 y | 全程上升 | 全腦類澱粉 |
| CSF p-tau181/Aβ42 | −14.0 y | 全程上升 | 液體 tau 活化 | |
| Mesial-T tau-PET | −11.9 y | 全程上升 | 內側顳葉 | |
| Temporo-parietal tau-PET | −11.7 y | 全程上升 | 側顳 / 頂葉 | |
| 血漿 Aβ42/40 | Roche Aβ42/40 | −14.4 y | −16.7 ~ −0.8 y 下降 | 最早異常 |
| C2N Aβ42/40 | −13.6 y | 同上 | — | |
| Fujirebio Aβ42/40 | −12.0 y | 同上 | — | |
| Quanterix Aβ42/40 | −8.4 y | 同上;+0 之後無顯著變動 | 顯著晚 | |
| p-tau / GFAP | ALZPath p-tau217 | −9.8y | 全程上升 | — |
| Janssen p-tau217 | −10.0 y | 全程上升 | — | |
| Fujirebio p-tau217 | −9.5 y | 全程上升 | — | |
| Roche p-tau181 | −9.4 y | 全程上升 | — | |
| Roche / Quanterix GFAP | −10.3 ~ −10.1 y | 全程上升 | 星狀膠細胞 | |
| 功能 / 結構 | CDR-SB | −6.2 y | 全程上升 | 功能下滑 |
| 皮質厚度 (Meta-ROI) | −2.1 y | 全程下降 | 結構萎縮 | |
| 神經退化 | Roche NfL | −4.3 y | 全程上升 | 晚期神經元損傷 |
| Quanterix NfL | −2.9 y | 全程上升 | 最遲異常 |
*負值 = 早於臨床症狀出現;正值 = 症狀之後。
本表由 ChatGPT 依據論文 Figure 4 與文字描述整理,僅供導讀參考。
| 生物標記 / 事件 | 首次達「異常」估計年份* | 臨床備註 | ||
|---|---|---|---|---|
| 類澱粉PET+ (Aβ-PET 0) |
Tau PET+ (tau-PET 0) |
症狀 (MCI or dementia 0 ) |
||
| C2N Aβ42/40 | −7.9 | −9.3 | −13.6 | 質譜;最早下降 |
| Roche Aβ42/40 | −7.9 | −9.0 | −14.4 | ECLIA 平台 |
| Fujirebio Aβ42/40 | −5.8 | −7.1 | −12.0 | CLEIA |
| Quanterix Aβ42/40 | −3.4 | -1.0 | −8.4 | Simoa;靈敏度最低 |
| 18F-FBP Aβ-PET | −5.9 | −7.8 | −14.4 | 斑塊堆積 |
| CSF p-tau181/Aβ42 | −5.2 | −7.4 | −14.0 | 液體 tau 活化 |
| Roche GFAP | −3.9 | −11.5 †† | −10.3 | 星狀膠細胞反應 |
| Quanterix GFAP | −3.5 | −10.0 | −10.1 | — |
| C2N %p-tau217 | −4.4 | −5.1 | −11.2 | 比例值;高敏 |
| C2N p-tau217 (濃度) | ≈0 | −4.7 | −9.4 | 濃度法 |
| ALZPath p-tau217 | −3.9 | −5.4 | −9.8 | — |
| Janssen p-tau217 | −3.2 | −4.9 | −10.0 | — |
| Fujirebio p-tau217 | −1.5 | −5.4 | −9.5 | 最晚異常的平台 |
| Roche p-tau181 | −2.9 | −6.7 | −9.4 | — |
| Quanterix p-tau181 | ≈0 | −5.4 | −8.5 | — |
| Mesial-T tau-PET 異常 | ≈0 | −4.7 | −11.9 | 內側顳葉 |
| TP tau-PET 異常 | +2.9 | −0.6 | −11.7 | 側顳 / 頂葉 |
| MRI Cortical thickness | +2.9 | −2.8 | −2.1 | 結構萎縮 |
| CDR-SB | 0 | −5.7 | −6.2 | 功能量表 |
| Roche NfL | +9.2 | +5.3 | −4.3 | 晚期神經損傷 |
| Quanterix NfL | +10.5 | +15.3 | −2.9 | 最終異常 |
*負值 = 早於時間軸 0 點;正值 = 晚於 0 點。
††Roche GFAP 點估 −11.5 y,但 95 % CI 與 Aβ42/40(−9 ~ −7 y)重疊,統計上未顯著更早。
本表格為 ChatGPT 依論文 Figure 4 之刻度與文字描述推估,僅供快速導讀參考。
討論
血漿生物標記物的異常時序與臨床應用潛力
-
此研究首次明確排序了 AD 血漿標記物相對於 amyloid PET、tau PET 與臨床症狀的異常時間點。
-
Aβ42/Aβ40 是最早出現異常的指標,約於症狀發作前 14 年變化,可作為早期篩選的工具。
-
但其生理濃度會進入平台期,限制了其在病程追蹤上的應用性。
-
相對地,p-tau217、p-tau181、GFAP 與 NfL 表現出持續上升趨勢,更適合用於疾病分期與療效監測。
🔎臨床意涵:
這些血漿標記的分時作用模式指出可建構多階段策略:先以 Aβ42/Aβ40 做篩檢,再利用 tau 類與 GFAP 評估進展風險與治療監控,最後以 NfL 判讀神經退化嚴重程度。
研究設計上的突破與與既有模型的比較
-
首次納入 tau PET 時鐘與症狀發作時間,創建三軸平行時間模型。
-
這種「疾病進展時間表(clock-based modeling)」策略,比傳統的「診斷分群」更能捕捉 AD 病程連續性。
-
優點包括:
-
可與不同測量平台對齊
-
適用於不同病理負荷狀態
-
強化生物標記之解釋效力
-
🔎理論貢獻:
將 PET 正位點作為對齊基準,能更精確描繪 preclinical-to-clinical transition,使 BBMs 在真實世界風險預測與精準介入中的角色更具可信度。
為何 tau PET 是預測症狀最好的時間指標?
-
研究發現 tau PET 陽性年齡與症狀發作年齡之間關聯最強(R² = 0.86),高於 amyloid PET(R² = 0.38)。
-
即使在同時納入 tau 與 amyloid PET 的模型中,只有 tau PET 仍是顯著因子。
-
這支持 tau 蛋白聚集比類澱粉沉積與臨床表現更具直接關聯。
-
儘管 ADNI 使用的是較敏感度較低的 PET,tau PET 仍展現出預測力,這也符合當前臨床與藥物開發重心逐漸轉向 tau 病理的趨勢。
🔎推論建議:
未來 AD 的預測與個人化時間軸建構應以 tau PET 為主軸,搭配血漿 p-tau 或 GFAP 作為替代指標進行可擴散性預測。
檢測平台差異的重要性:非技術性偏差的主因
-
同一標記物在不同平台上的變異性顯著。
-
例如 Quanterix 的 Aβ42/Aβ40 變化時間明顯晚於 C2N 或 Roche,解釋了其與 amyloid PET 的關聯性較低。
-
C2N 的 %p-tau217 早於其單測ptau 217,可能因減少慢性腎病等干擾因素的影響。
-
-
這些差異不僅來自檢測靈敏度,還包括:分子特異性、樣本處理、背景雜訊與抗體特異性。
🔎實務重點:
臨床與研究應避免不同平台間的數據混用,並應根據需求選用靈敏度與適用期程最佳的組合平台與標記物。
研究限制與未來挑戰
-
時間預估模型以相對保守的 PET 陽性閾值為基準,可能低估部分早期病理變化。
-
tau PET 陽性標準以 mesial-temporal ROI 為主,較易受非 AD tauopathy(如 PART 或老化)干擾。
-
預測症狀年齡的模型僅基於 17 位 clinical converters,需擴大樣本驗證。
-
樣本族群以白人、高學歷者為主,代表性有限。
-
不同平台在靈敏度與應用領域上的差異,需更大規模交叉驗證。
🔎建議:
未來研究應納入更廣泛族群(種族、教育程度、社會決定因子)
-
建立跨平台標準化轉換指標
-
結合多模態標記(如:neuroinflammation、microstructural MRI)以強化疾病進展模型的預測準確度
個人總結 & 批判
研究採用 GAM-LMM,為 Aβ 與 tau 各建一條「生物鐘」,首度把 30 多項生物標記在三條時間軸上的先後順序精確量化。
Aβ42/40 最先下降,隨後 GFAP 與 p-tau 迅速上升,速度與 tau 病理擴散幾乎同步;NfL 則在病程相當後期才顯著升高。
六種檢測平台測到同一指標的「異常點」最多可相差 4–6 年,跨平台使用前必須謹慎校正。
模型外推假設變化呈線性,恐漏掉真實的 S 型(sigmoidal)轉折。
Tau-PET 閥值設在 Braak I/II 區域,可能混入正常老化的 tau 訊號。
症狀進展樣本僅 17 人,統計效力有限,需小心解讀。
需注意在tau時間軸,GFAP 的點估雖與 Aβ42/40 的 95 % CI 重疊,卻因平均值而被標示為「最早」,有高估之虞,代表這個值的變異很大,也有可能和tau PET陽性者可能合併有其它tau病變相關。
若未來加入 TSPO-PET(微膠細胞活化)或 FDG-PET(腦代謝)軸線,仍需再次驗證 GFAP 與 p-tau 的時序是否依舊成立。
1️⃣ Amyloid-related 指標
| 指標 / 平台 | Aβ-PET+ | Tau PET+ | >=MCI |
|---|---|---|---|
| C2N Aβ42/40 | −7.9 | −9.3 | −13.6 |
| Roche Aβ42/40 | −7.9 | −9.0 | −14.4 |
| Fujirebio Aβ42/40 | −5.8 | −7.1 | −12.0 |
| Quanterix Aβ42/40 | −3.4 | -1.0 | −8.4 |
| 18F-FBP Aβ-PET | −5.9 | −7.8 | −14.4 |
2️⃣ p-tau-related 指標
| 指標 / 平台 | Aβ-PET+ | Tau PET+ | >=MCI |
|---|---|---|---|
| CSF p-tau181/Aβ42 | −5.2 | −7.4 | −14.0 |
| C2N %p-tau217 | −4.4 | −5.1 | −11.2 |
| C2N p-tau217 (濃度) | ≈0 | −4.7 | −9.4 |
| ALZPath p-tau217 | −3.9 | −5.4 | −9.8 |
| Janssen p-tau217 | −3.2 | −4.9 | −10.0 |
| Fujirebio p-tau217 | −1.5 | −5.4 | −9.5 |
| Roche p-tau181 | −2.9 | −6.7 | −9.4 |
| Quanterix p-tau181 | ≈0 | −5.4 | −8.5 |
3️⃣ Tau-PET 指標
| 指標 / 平台 | Aβ-PET+ | Tau PET+ | >=MCI |
|---|---|---|---|
| Mesial-T tau-PET 異常 | ≈0 | −4.7 | −11.9 |
| Temporo-parietal tau-PET 異常 | +2.9 | −0.6 | −11.7 |
4️⃣ 其他(GFAP/NfL/功能量表等)
| 指標 / 平台 | Aβ-PET+ | Tau PET+ | >=MCI |
|---|---|---|---|
| Roche GFAP | −3.9 | −11.5 †† | −10.3 |
| Quanterix GFAP | −3.5 | −10.0 | −10.1 |
| CDR-SB | 0 | −5.7 | −6.2 |
| MRI Cortical thickness | +2.9 | −2.8 | −2.1 |
| Roche NfL | +9.2 | +5.3 | −4.3 |
| Quanterix NfL | +10.5 | +15.3 | −2.9 |
*負值=早於時間軸 0 點;正值=晚於 0 點。
††Roche GFAP 點估 −11.5 y,但其 95 % CI 與 Aβ42/40(−9 ~ −7 y)重疊,統計上未顯著更早。
本四表格由 ChatGPT 依論文 Fig 4 視覺刻度與文字描述推算,僅供快速導讀參考。
重點問答
Q1. 為何要用「類澱粉鐘」與「tau 鐘」對齊血漿指標?
本研究最大貢獻在於把抽血數據精準映射到腦內病理時序。研究者先以 ADNI 784 例類澱粉、359 例 tau PET 建兩條「生物鐘」,再將 292 人三次血檢重置到同一軸線,明確標註各血漿指標從正常到異常的年份。透過將 PET 陽性點設為零時點,可一眼看出 Aβ42/Aβ40、GFAP、p-tau 與 NfL 的領先或滯後幅度,為超早期篩檢、疾病分期與藥效監控提供量化座標,彌補過往只知先後順序、難以估算「差幾年」的臨床痛點。
Q2. 在類澱粉時間軸上,哪個指標最早異常?血漿還是PET?提早多少?
質譜 C2N 與 Roche 測得的 Aβ42/Aβ40 比值最先下降,領先類澱粉 PET 陽性 7.9 年、臨床症狀 14.4 年;Fujirebio 早 5.8 年,Quanterix 僅早 3.4 年。曲線於陽性後 11–13 年趨平,適合用於「超早期篩選」,卻不利長期分期。平台靈敏度差異意味若使用較遲異常的平台,可能漏掉真正早期個案;此外,該降幅幾乎同步於 26 Centiloid 以下微量斑塊堆積,顯示血檢可在影像之前捕捉病程起跑點,對預防試驗收案尤關鍵。
Q3. 在 tau 時間軸中,GFAP 與 p-tau 的先後順序透露什麼病理訊息?
GFAP 於 tau PET 陽性前約 11.5 年率先升高,反映星狀細胞對早期 tau 或神經發炎的敏感反應;之後 p-tau217 與 p-tau181 在 −6.7 至 −4.7 年快速攀升,且全程線性增加。雖信賴區間部分重疊,但功能定位分明:GFAP 像「病理啟動燈」,而 p-tau 系列是「活動性刻度」,最適合用來評估藥效與分期。須注意研究以 mesial-temporal SUVR 1.41 為閾值,可能混入年齡相關 tauopathy,故實際領先幅度可能更大。
Q4. 預測臨床症狀時,哪個里程碑最可靠?
線性回歸顯示,達到 tau PET 陽性的年齡可單獨解釋認知症狀年齡 86% 變異(R² = 0.86),而類澱粉 PET 陽性年齡僅解釋 38%。雙變項模型下唯有 tau 仍顯著,APOE 與性別皆無額外貢獻,證明臨床轉折真正由 tau 累積驅動。此預測力與家族性 AD 研究相當,支持「tau 驅動學說」,並提示治療與追蹤應聚焦 tau 早期上升段,而非等待斑塊大量沉積後才介入。
Q5. 同一指標換檢測平台為何會改寫時間軸?臨床該如何解讀?
平台差異源於抗體特異度、目標分子型態與雜訊處理:質譜 C2N 與 Roche 的 Aβ42/Aβ40 提早 7.9 年異常,Quanterix 延遲至 3.4 年;C2N %p-tau217 則比單獨測ptau217提早 4.4 年升高。若未掌握各平台基準,可能將早期患者判為正常或在共病狀況下誤認假陽性。作者建議先建立「平台對照年表」,依研究目的選擇合適靈敏度,再將結果用於篩檢與分期;未來指南亦宜標註各平台臨界值與建議用途,以免跨中心比較時產生解讀落差。